Phản ứng nhiệt nhôm là một quá trình hóa học có tầm quan trọng không thể bỏ qua trong nghiên cứu hóa học chuyên ngành. Đây là một phản ứng có vẻ quen thuộc nhưng đồng thời lại đầy bí ẩn. Mặc dù nhôm luôn góp mặt trong phản ứng này, nhưng liệu còn những yếu tố hóa học nào khác tham gia? Và phản ứng nhiệt nhôm có ứng dụng gì trong cuộc sống hàng ngày? Bài viết ngày hôm nay sẽ sát cánh bạn bước vào thế giới của phản ứng nhiệt nhôm, để làm rõ những câu hỏi này và khám phá những ứng dụng thú vị.
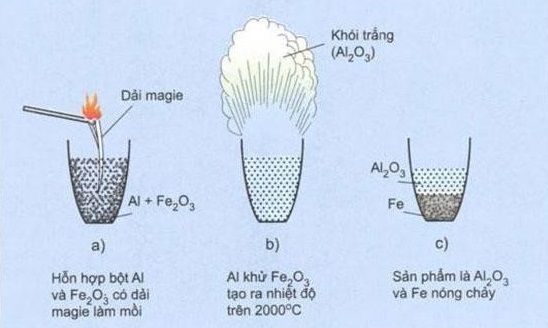
Hình ảnh phản ứng nhiệt nhôm trong PTN
1. Phản ứng nhiệt nhôm là gì?
Phản ứng nhiệt nhôm là một quá trình hóa học nổi tiếng với sự tỏa nhiệt mạnh mẽ, trong đó nhôm đóng vai trò quan trọng như một chất khử. Nói một cách đơn giản, đây là một loại phản ứng thường xảy ra giữa nhôm và các oxit kim loại, dẫn đến sự tạo thành kim loại và nhôm oxit.
Một ví dụ phổ biến và rất nổi tiếng về phản ứng nhiệt nhôm là phản ứng giữa nhôm và oxit sắt, được biểu thị bằng phương trình:
Fe2O3 + 2Al → 2Fe + Al2O3
Hoặc chúng ta có thể viết lại phương trình này dưới dạng tổng quát:
2yAl + 3FexOy → yAl2O3 + 3xFe
Ngoài ra, có một số phản ứng khác cũng quan trọng và thú vị như:
- 3CuO + 2Al → Al2O3 + 3Cu
- 8Al + 3Fe3O4 → 4Al2O3 + 9Fe
- 3Mn3O4 + 8Al → 4Al2O3 + 9Mn
- Cr2O3 + 2Al → Al2O3 + 2Cr
Tất cả các phản ứng này đều thuộc loại phản ứng oxi hóa khử, trong đó nhôm là chất khử và các oxit kim loại là chất oxi hóa. Trong quá trình này, các chất oxi hóa bị giảm đi và chất khử là nhôm sẽ được oxi hóa, đồng thời tạo ra nhiệt độ cao và sản phẩm cuối cùng là kim loại và nhôm oxit.
Xem thêm:
2. Đặc điểm và ứng dụng của phản ứng nhiệt nhôm
2.1. Đặc điểm của PƯ nhiệt nhôm
Phản ứng nhiệt nhôm là một quy trình độc đáo, được áp dụng lần đầu để khử các oxit kim loại mà không cần sử dụng cacbon như trong các phản ứng khử thông thường. Đặc trưng của phản ứng này là sự tỏa nhiệt mạnh mẽ, nhưng cũng đòi hỏi một lượng năng lượng hoạt hóa đáng kể để vượt qua sự phá vỡ các liên kết nguyên tử, bao gồm cả liên kết kim loại.
Trong PƯ nhiệt nhôm, nhôm được đun nóng cùng với các oxit kim loại trong một lò đốt. Để đảm bảo quá trình diễn ra một cách hiệu quả, nhôm và các oxit kim loại được nghiền thành bột và sau đó trộn chung để tạo thành một hỗn hợp. Quá trình này đã được Hans Goldchmidt phát triển và đã được bảo hộ bằng bằng sáng chế từ năm 1898.
Xem thêm:
2.2. Ứng dụng của PƯ nhiệt nhôm
Ứng dụng chính của phản ứng nhiệt nhôm nổi tiếng nhất là trong việc hàn và vá đường ray cho tàu hỏa. Sự tỏa nhiệt mạnh mẽ của phản ứng này giúp nối lại và làm chắc chắn các đoạn đường ray, tạo ra mối nối vững chắc và an toàn.

Ứng dụng của phản ứng nhiệt nhôm
Ngoài ra, phản ứng này còn được sử dụng để khử oxit của các kim loại yếu hơn trong dãy hoạt động hóa học của kim loại. Ứng dụng này có thể bao gồm việc tạo ra các hợp kim kim loại đặc biệt.
Phản ứng nhiệt nhôm cũng đóng vai trò quan trọng trong việc sản xuất nhiều hợp kim sắt, như ferroniobium từ niobium pentoxide và ferrovanadium (FeV) từ Vanadi oxide (V2O5).
Như vậy, phản ứng nhiệt nhôm không chỉ là một hiện tượng hóa học thú vị mà còn có những ứng dụng quan trọng và đa dạng trong nhiều lĩnh vực.
3. Lý thuyết phản ứng nhiệt nhôm
3.1. Các trường hợp của phản ứng
Hãy tưởng tượng một hỗn hợp X, bao gồm nhôm và một oxit kim loại nào đó, tham gia vào một phản ứng và tạo ra một hỗn hợp mới, được gọi là Y. Trong trường hợp này, có hai kịch bản có thể xảy ra: phản ứng hoàn toàn và phản ứng không hoàn toàn.
Phản ứng xảy ra hoàn toàn
Nếu phản ứng diễn ra hoàn toàn, một số câu hỏi có thể được đặt ra:
- Hỗn hợp Y bao gồm cả hai kim loại: Nhôm còn dư, kim loại mới tạo ra và không còn oxit kim loại.
- Hỗn hợp Y có khả năng phản ứng với dung dịch kiềm, tạo ra khí H2 và chứng tỏ sự còn dư của nhôm.
- Hỗn hợp Y tác dụng với dung dịch axit, sản xuất khí và có thể chứa một hỗn hợp gồm (Al2O3 và kim loại mới), (Al2O3, Al và kim loại mới), hoặc (Al2O3, kim loại mới và oxit kim loại còn thừa).
Phản ứng xảy ra không hoàn toàn
Trong trường hợp phản ứng không diễn ra hoàn toàn, hỗn hợp Y sẽ bao gồm nhôm dư, Al2O3, oxit kim loại còn dư và kim loại mới tạo ra.
3.2. Định luật liên quan đến PƯ nhiệt nhôm
Phản ứng nhiệt nhôm tuân theo định luật bảo toàn khối lượng và định luật bảo toàn nguyên tố (mol nguyên tử).
- Khối lượng hỗn hợp X (mhhX) bằng khối lượng hỗn hợp Y (mhhY).
- Số mol của kim loại Fe trong X (nFe(X)) bằng số mol của kim loại Fe trong Y (nFe(Y)), và số mol của nhôm Al trong X (nAl(X)) bằng số mol của nhôm Al trong Y (nAl(Y)).
mhhX = mhhY
nFe(X) = nFe(Y) và nAl(X) = nAl(Y)
4. Cách giải bài tập phản ứng nhiệt nhôm
Khi tiến hành giải các bài tập, đề xuất một số lưu ý quan trọng dưới đây:
Nếu sau phản ứng hỗn hợp tạo ra khí hidro (H2) khi tác dụng với dung dịch kiềm, điều này cho thấy có sự còn dư của nhôm (Al) hoặc hiệu suất phản ứng không đạt 100%. Trong trường hợp này, nhôm dư sẽ tiếp tục phản ứng với kiềm, tạo thành sản phẩm theo phản ứng hóa học sau đây (ví dụ với NaOH):2Al + 2H2O + 2NaOH → 2NaAlO2 + 3H2↑
Nếu sau phản ứng hỗn hợp không tạo ra khí hidro (H2) khi tác dụng với dung dịch kiềm, điều này chỉ ra rằng nhôm đã phản ứng hết và phản ứng đã diễn ra hoàn toàn.
Trong trường hợp đề bài yêu cầu phản ứng xảy ra hoàn toàn, chắc chắn sẽ tạo ra nhôm oxit (Al2O3) và kim loại mới. Tuy nhiên, nhôm hoặc oxit kim loại có thể còn dư, vì vậy cần chú ý đến điều này trong quá trình giải bài tập.
Khi giải bài tập, bạn có thể áp dụng định luật bảo toàn khối lượng hoặc định luật bảo toàn electron để giải quyết các vấn đề liên quan đến phản ứng.
5. Giải đáp câu hỏi về phản ứng nhiệt nhôm
Câu 1: Phản ứng nào sau đây là phản ứng nhiệt nhôm
- A. 2Al + 3H2SO4 → Al2(SO4)3 + 3H2.
- B. 2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2.
- C. 3FeO + 2Al → 3Fe + Al2O3.
- D. 2Al + 3CuSO4 → Al2(SO4)3 + 3Cu.
Đáp án: C
Câu 2: Phản ứng nào sau đây không phải là phản ứng nhiệt nhôm
- A. Al tác dụng với H2SO4 đặc, nóng.
- B. Al tác dụng với CuO nung nóng.
- C. Al tác dụng với Fe2O3 nung nóng.
- D. Al tác dụng với Fe3O4 nung nóng.
Đáp án: A
Câu 3: Kim loại nào sau đây có thể điều chế được bằng phản ứng nhiệt nhôm
- A. Na
- B. Fe
- C. Ca
- D. Al
Đáp án B. Điều chế kim loại bằng phản ứng nhiệt nhôm từ những kim loại đứng sau nhôm như Fe. Còn Na, Ca, Al không phải là đáp án đúng.
6. Lời kết
Tóm lại, phản ứng nhiệt nhôm không chỉ là một khám phá hóa học đầy ý nghĩa, mà còn là một công cụ quan trọng trong ngành sản xuất và công nghiệp. Khả năng sử dụng nhôm như một chất khử để khắc phục các oxit kim loại đã đem lại sự đột phá trong quá trình này. Phản ứng này, mặc dù tỏa nhiều nhiệt, nhưng đòi hỏi một lượng năng lượng khởi đầu, và chúng ta cần chú ý đến sản phẩm cuối cùng để giải quyết bài tập một cách chính xác.
Hãy ghi nhớ những phương trình hóa học và kiến thức từ bài viết này, vì chúng có thể hữu ích trong tương lai khi bạn tiếp tục khám phá hóa học chuyên ngành.








![Tất cả các Công Thức Đạo Hàm đầy đủ nhất [Full]](https://hoconlinemienphi.com/wp-content/uploads/2025/03/cong-thuc-dao-ham-120x86.jpg)






